杭州铂赛生物科技有限公司
7 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.9000000000000004
- 0.9000000000000004
- 1.9000000000000004
- 0.9000000000000004
工程化外泌体/外泌体工程化修饰/外泌体表征
询价
杭州铂赛生物科技有限公司
入驻年限:7 年
- 联系人:
蔡老师
- 所在地区:
浙江 杭州市 滨江区
- 业务范围:
技术服务、原辅料包材、体外诊断、耗材、实验室仪器 / 设备、医疗器械、书籍 / 软件
- 经营模式:
医院药店 生产厂商 经销商 代理商
公司新闻/正文
看过不后悔的科研新方向,一种重要的翻译后新修饰—PARylation,或将延续“乳酸化”的研究传奇~
1104 人阅读发布时间:2025-06-27 17:23
老套路走出新传奇,今天让我们站在「乳酸化」的肩膀上看这种重要的翻译后新修饰:多聚ADP-核糖基化修饰(PARylation)。
自乳酸化、泛素化、磷酸化 、糖基化、甲基化、乙酰化等多种经典的蛋白质翻译后修饰相继爆火出圈后,新的蛋白质翻译后修饰类型还在不断涌现。据说目前已经发现有600多种蛋白质翻译后修饰类型,今天小编就为大家带来一个新鲜热点修饰方式—多聚ADP-核糖基化修饰(PARylation:Poly(ADP-ribosyl)ation)。
目前PARylation的文章数量呈现逐年增加的趋势,创新性较高,一般都是一区/二区的水准。不仅在临床研究方面多有应用,也非常适合做国自然课题。
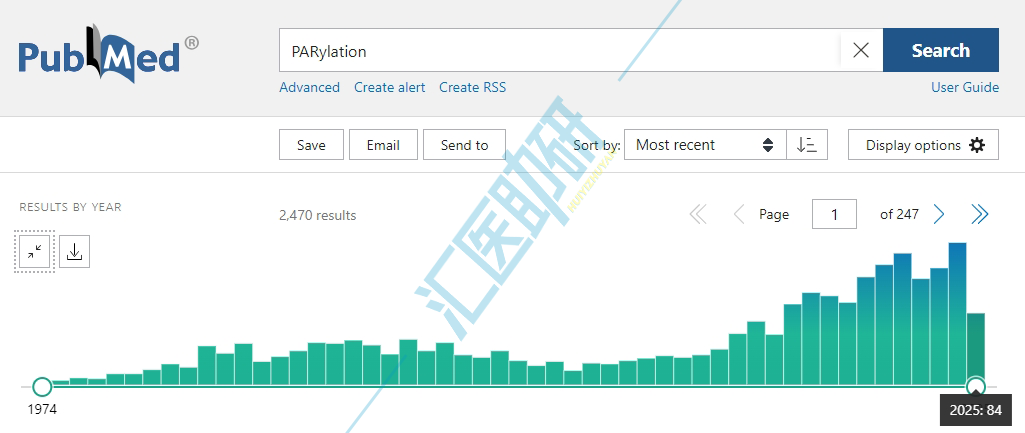
都说做新不如做熟,但好的研究是方向新套路熟,带着乳酸化研究的「经典套路」探索新方向—PARylation,深入解析临床新的分子机制和细胞功能!不确定课题是否适用该方向,右上角直接联系,专业的预测网站,为您预测ADP核糖基化位点,规划相关的高水准课题!
往下翻↓,让我们先来了解一下多聚ADP-核糖基化修饰的相关基础知识!
多聚ADP-核糖基化修饰
PARylation是一种翻译后修饰过程,由PARP酶家族催化,将多个NAD衍生的ADP -核糖(ADPr )单元连接到受体蛋白上。PARylation可以调节蛋白质生物合成过程。PARP1是PARP家族中最丰富的成员,被认为是“原型” PARP酶,利用烟酰胺腺嘌呤二核苷酸(NAD+)作为共底物催化PARylation。
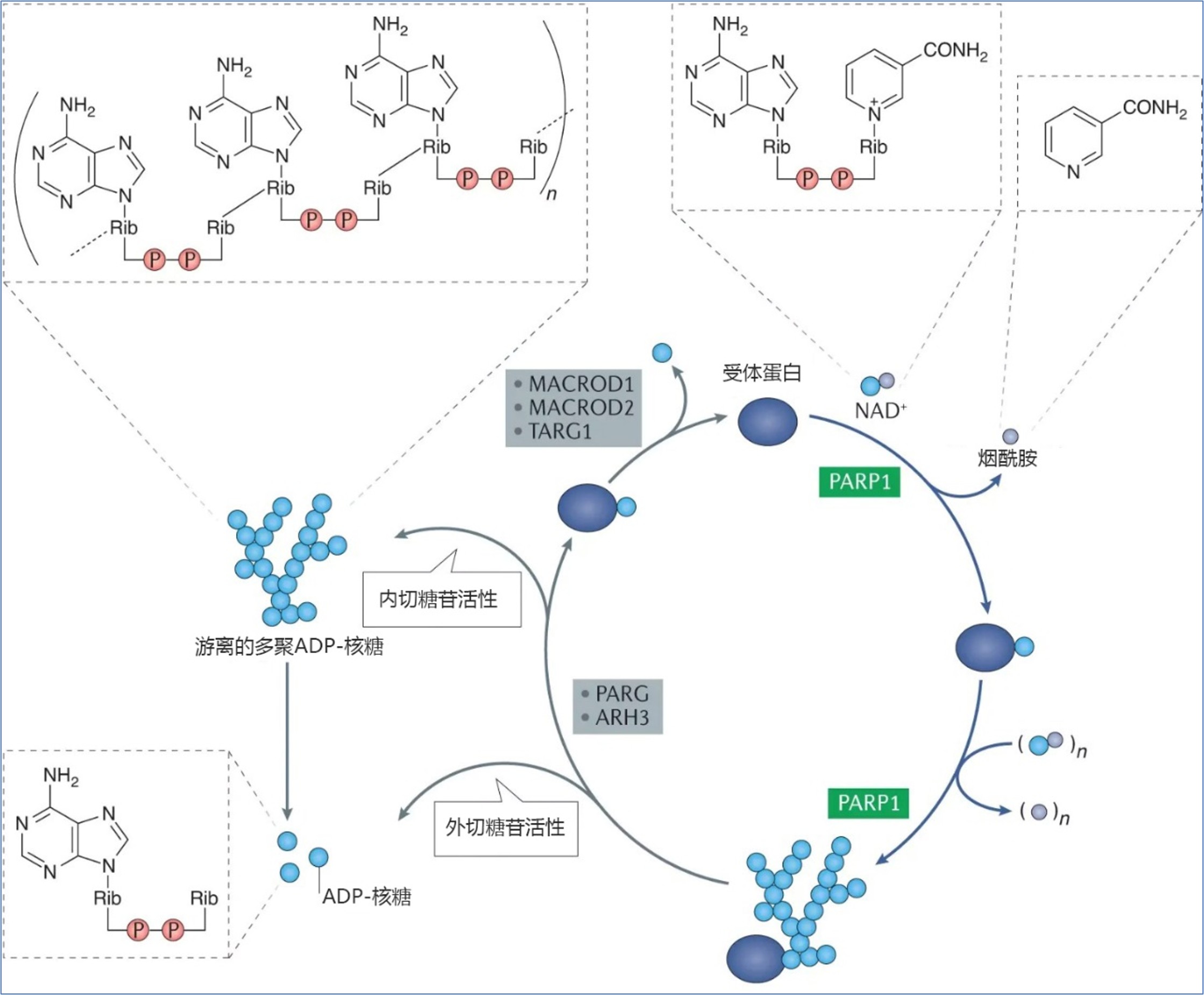
PARylation分类
根据ADP-核糖(PAR)单元的数量可分为三类:
-
单PAR化(MARylation,单个ADP-核糖修饰)
-
寡聚PAR化(oligo PARylation)
-
多聚PAR化(poly PARylation)
PARP家族成员
人类17/小鼠16个成员:
PARP-1、PARP-2、PARP-5a和PARP-5b可催化形成多聚PAR化修饰,而其他PARP成员(除PARP-9和PARP-13外)主要在细胞核或细胞质中诱导单PAR化修饰。
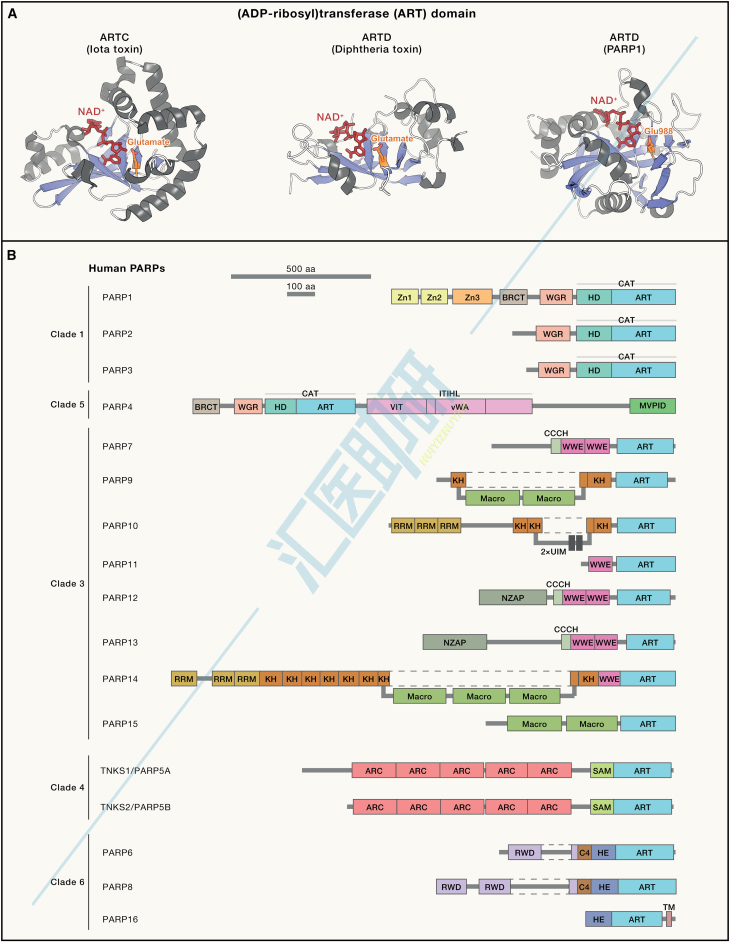
PARylation生理功能
多聚ADP-核糖基化(PARylation)是ADP-核糖基化的一种,也是一种动态可逆的PTM(翻译后修饰)系统,借用表观遗传调控中常用的说法,有一套writer、reader、eraser等酶系进行调控。writer即催化形成ADP-核糖化修饰的酶,统称为ADP-核糖基转移酶((ADP-ribosyl)transferases,ARTs),是一类具有单或多ADP-核糖基转移活性的蛋白质。
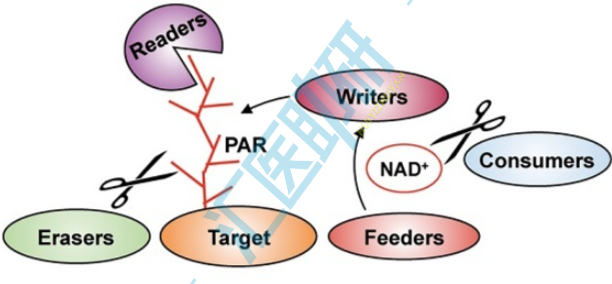
ADP-核糖基化可以改变蛋白质的活性、稳定性和配体结合能力,这与多种疾病的发生和发展密切相关,在调控细胞功能和应对外界挑战中发挥着重要作用。在DNA修复、转录调控、细胞周期调控、免疫应答等多种生物学过程中,扮演着至关重要的角色。
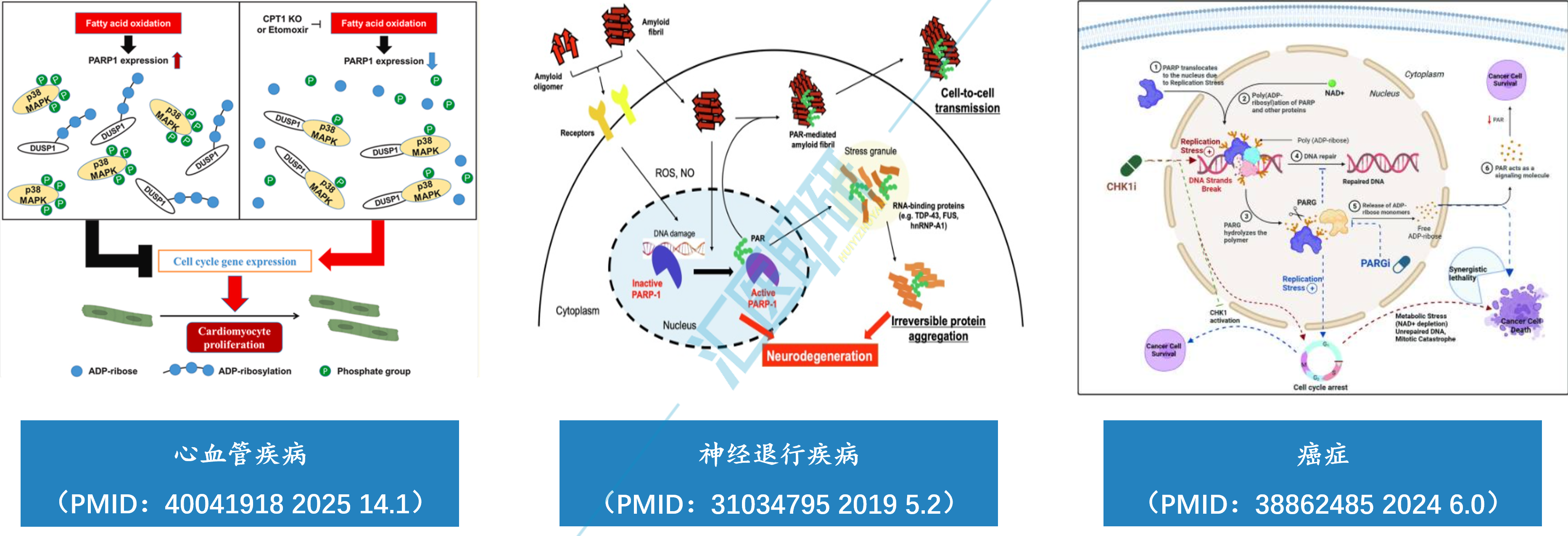
-
心血管疾病,如血管钙化、动脉粥样硬化、心肌梗死等;
-
神经退行性疾病,如肌萎缩侧索硬化症(ALS)、阿尔茨海默病(AD)等;
-
免疫与代谢性疾病,如自身免疫病,糖尿病并发症等;
-
炎症性疾病,如特异性皮炎、炎症性肠病等;
-
癌症,如卵巢癌、结直肠癌、食管鳞状细胞癌等。
在DNA损伤应答和修复中的作用
PARP-1是一种DNA损伤感应蛋白,可将带负电荷的PAR连接到自身或靶蛋白上。这一过程涉及DNA损伤下细胞内大量NAD+的消耗。多聚ADP核糖基化在DDR和DNA修复途径中具有多种作用,包括单链断裂、双链断裂、DNA复制叉和染色质结构的修复。
在炎症调控中的作用
炎症反应发生在各种环境中,例如在肿瘤、病毒感染、代谢性疾病和神经退行性疾病中;它们常常伴随着多聚ADP核糖基化。多聚ADP核糖基化调节诱导型一氧化氮合酶的水平,PARP抑制剂抑制多聚ADP核糖基化和iNOS的表达,参与全身炎症反应。
在代谢调控中的作用
多聚ADP核糖基化可以直接和间接调控细胞和全身代谢。由于多聚ADP核糖基化是细胞应激的指标,因此组织或细胞中多聚ADP核糖基化的增加是代谢异常状态的代表。此外,多聚ADP核糖基化是NAD +/NADH水平的指示剂,可用于细胞能量感知和信号传导。
在细胞死亡中的作用
应激原诱导的DNA损伤诱导多聚ADP核糖基化,合成的PAR招募DNA修复蛋白复合物到DNA损伤区域。由于hyper-多聚ADP核糖基化引起的一系列过程,广泛的DNA损伤可导致细胞死亡。
PARylation相关研究案例
案例一
为了探究代谢重编程(糖酵解→脂肪酸氧化)能否调控心肌细胞增殖,并解析CPT1抑制促再生的分子机制。第三军医大学大坪医院团队构建心脏特异性Cpt1a/b双敲小鼠,结合依托莫克西(CPT1抑制剂)处理,通过RNA测序、代谢组学及p38 MAPK磷酸化分析验证机制。发现CPT1抑制(依托莫克西或基因敲除)逆转代谢重编程,通过减少PARP1介导的DUSP1蛋白PARylation,降低p38 MAPK磷酸化水平,显著激活成年心肌细胞增殖并促进心梗后心脏再生,证实代谢干预是心脏修复的有效策略。

案例二
为了探究PARP1介导的PARylation修饰能否调控VSMC铁死亡及其在血管钙化中的作用。东南大学附属中大医院团队通过构建Parp1flox/flox Tagln Cre+小鼠模型,结合β-甘油磷酸处理VSMC,利用RNA测序及POLG敲低验证分子机制。发现PARP1介导POLG的PARylation修饰触发了其泛素化降解,导致线粒体功能障碍并激活Adora2a/Rap1信号通路,诱导VSMC铁死亡及血管钙化,抑制PARP1可逆转该过程,提示PARP1抑制剂具治疗潜力。
案例三
为了探究NUDT13是如何通过抑制PKM1的PARylation修饰调控结直肠癌(CRC)代谢重编程及肿瘤发生机制。中山大学研究团队通过转录组分析、Nudt13时空敲除小鼠模型、PARP1抑制剂Olaparib处理及模拟肽段功能验证。发现NUDT13通过抑制PARP1介导的PKM1 PARylation,稳定PKM1蛋白并诱导CRC细胞氧化磷酸化表型,显著抑制肿瘤发生;靶向Nudix基序的模拟肽可阻断CRC进展。

常规服务:PARylation的检测
-
主要检测方法为免疫共沉淀Co-IP;

研究无思路、模型难关联、分析不会搞,实验没资源,但又想开展这方面的课题研究,右上角直接联系客服~可根据您的研究方向为您量身定制相关课题,助力您的研究成果快速落地~






