杭州铂赛生物科技有限公司
7 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.9000000000000004
- 0.9000000000000004
- 1.9000000000000004
- 0.9000000000000004
液-液相分离(LLPS)/无膜细胞器研究
询价
杭州铂赛生物科技有限公司
入驻年限:7 年
- 联系人:
蔡老师
- 所在地区:
浙江 杭州市 滨江区
- 业务范围:
技术服务、原辅料包材、体外诊断、耗材、实验室仪器 / 设备、医疗器械、书籍 / 软件
- 经营模式:
医院药店 生产厂商 经销商 代理商
公司新闻/正文
中科大附一院肝癌研究重大突破!从临床发现到分子机制再到靶点干预,Nature Cancer揭秘液-液相分离(LLPS)新靶点!
248 人阅读发布时间:2025-06-17 17:06
由液-液相分离(LLPS)形成的无膜细胞器—应激颗粒(SGs),对于应激反应至关重要,它能够暂时储存mRNA,在时间和空间上以动态且可逆的方式进行相关调节,阻止不必要的蛋白质翻译,帮助细胞优先应对应激。目前,多项研究发现癌细胞利用不同的应激颗粒相关机制来克服环境和治疗带来的损伤。
肝癌(HCC)是全球癌症相关死亡的第三大原因,酪氨酸激酶抑制剂(TKIs)的耐药性严重限制了其临床疗效。肝癌微环境中的营养匮乏、氧化应激等胁迫条件迫使肿瘤细胞激活适应性机制,其中应激颗粒(SGs)作为无膜细胞器,通过相分离动态调控mRNA翻译,但其在肝癌中的作用尚不明确。
近日,中国科学技术大学附属第一医院(安徽省立医院)刘连新、王继洲、宋瑞鹏、张树庚、王嘉倍等人共同在《Nature Cancer》期刊发表论文“RIOK1 phase separation restricts PTEN translation via stress granules activating tumor growth in hepatocellular carcinoma”,本研究揭示了非典型激酶RIOK1通过液-液相分离(LLPS)形成应激颗粒(SGs),抑制PTEN翻译并激活磷酸戊糖途径(PPP),从而驱动肝癌进展和TKI耐药的机制。

研究思路
采用"临床问题-分子机制-治疗策略"的研究路径:
-
首先通过临床样本分析和数据库挖掘,发现RIOK1在肝癌中异常高表达且与不良预后相关;
-
随后运用多组学技术,系统解析RIOK1通过液-液相分离(LLPS)调控应激颗粒形成的分子机制;
-
最终基于机制研究结果,开发靶向干预策略并验证其治疗效果。
这项研究从临床问题出发,通过系统的机制研究,最终回到临床转化,体现了转化医学研究的完整闭环。不仅为理解肝癌耐药提供了新视角,更重要的是发现了可快速临床转化的治疗策略。
细胞质中的应激颗粒(SGs)是通过多价蛋白质与 RNA 之间的相互作用经液-液相分离(LLPS)形成的无膜细胞器。对体内微环境的应激反应起到至关重要的作用,与多种疾病的发生相关,特别是在细胞应激领域,LLPS绝对是一个不容错过的新领域。
关键发现
-
RIOK1与HCC进展相关:RIOK1在HCC中的高表达与患者预后不良相关,并且与NRF2的转录激活有关。
-
RIOK1通过相分离限制PTEN翻译:RIOK1通过与IGF2BP1和G3BP1相互作用,将PTEN mRNA纳入应激颗粒,从而抑制PTEN的翻译。
-
RIOK1激活磷酸戊糖途径(PPP):RIOK1的表达与PPP的激活相关,这有助于细胞应激解决和对TKI的保护。
-
Chidamide作为RIOK1小分子抑制剂:Chidamide能下调RIOK1的表达,并增强TKI的疗效,为HCC治疗提供了新的策略。
结果图示
1、高RIOK1表达与肝细胞癌进展相关
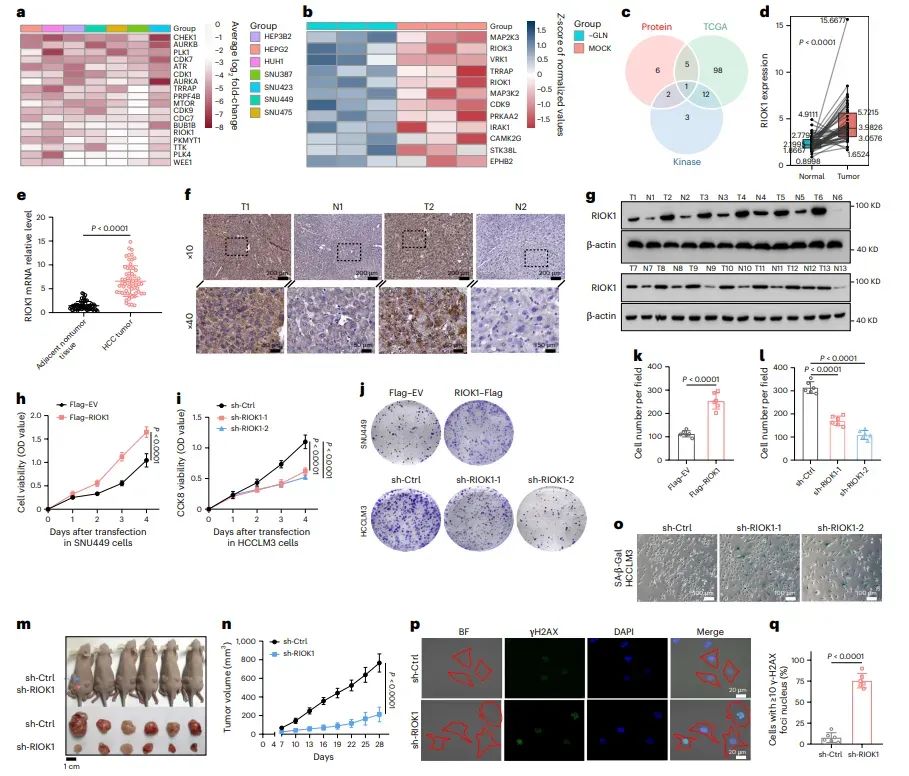
2、RIOK1通过IGF2BP1与G3BP1的相互作用驱动应激颗粒的组装
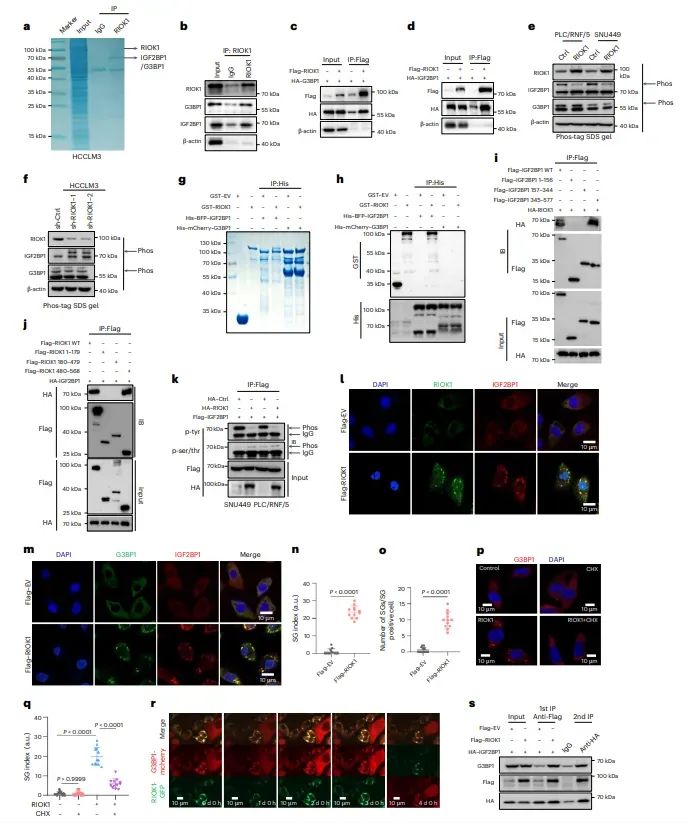
3、RIOK1 在体内和体外均会发生液-液相分离(LLPS)
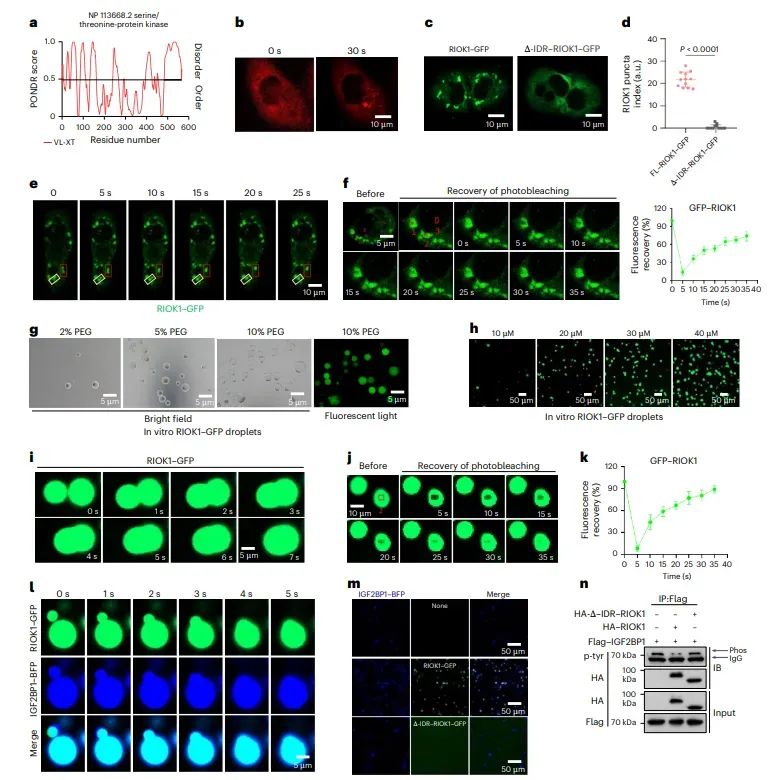
4、RIOK1 LLPS抑制 PTEN 翻译
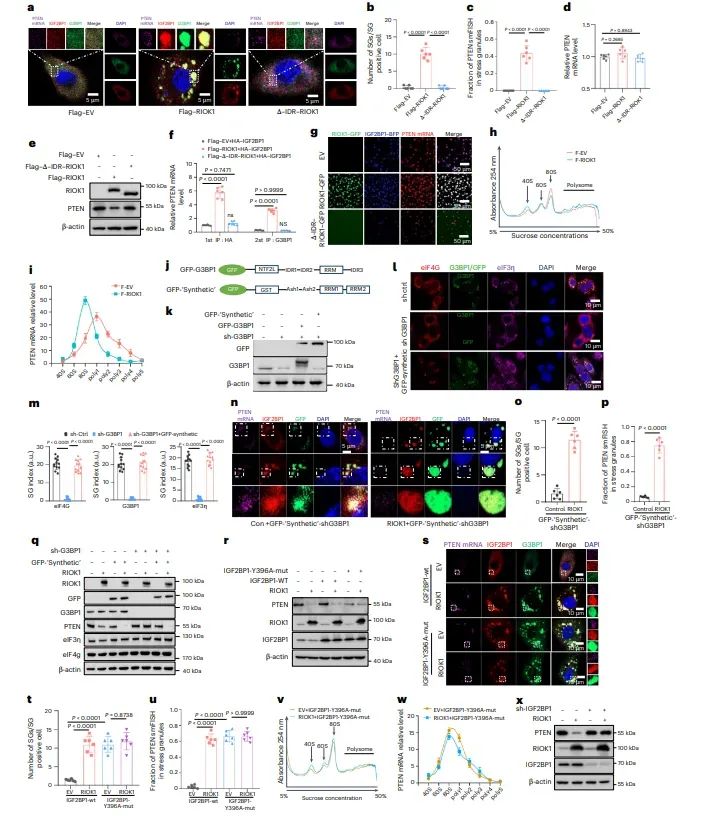
5、RIOK1促进磷酸戊糖途径并由NRF2转激活
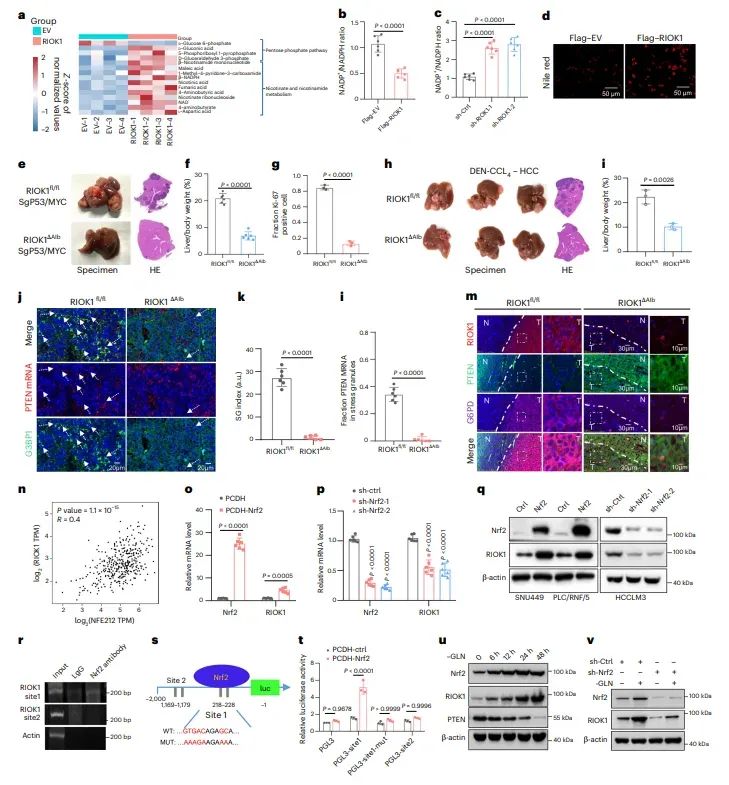
6、RIOK1诱导的LLPS会降低肝细胞癌对酪氨酸激酶抑制剂的敏感性
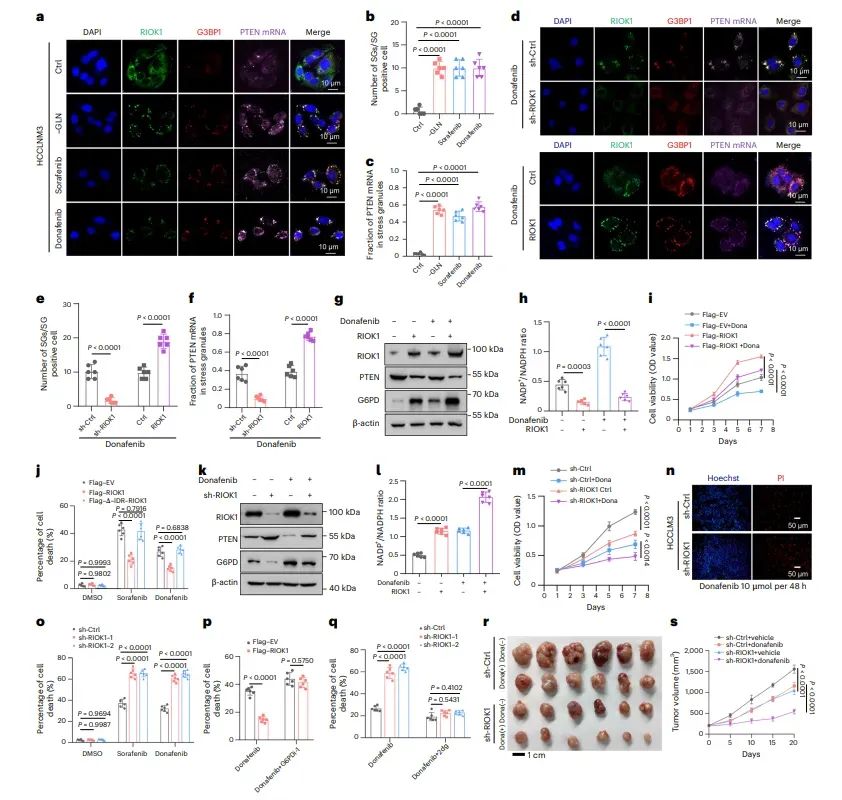
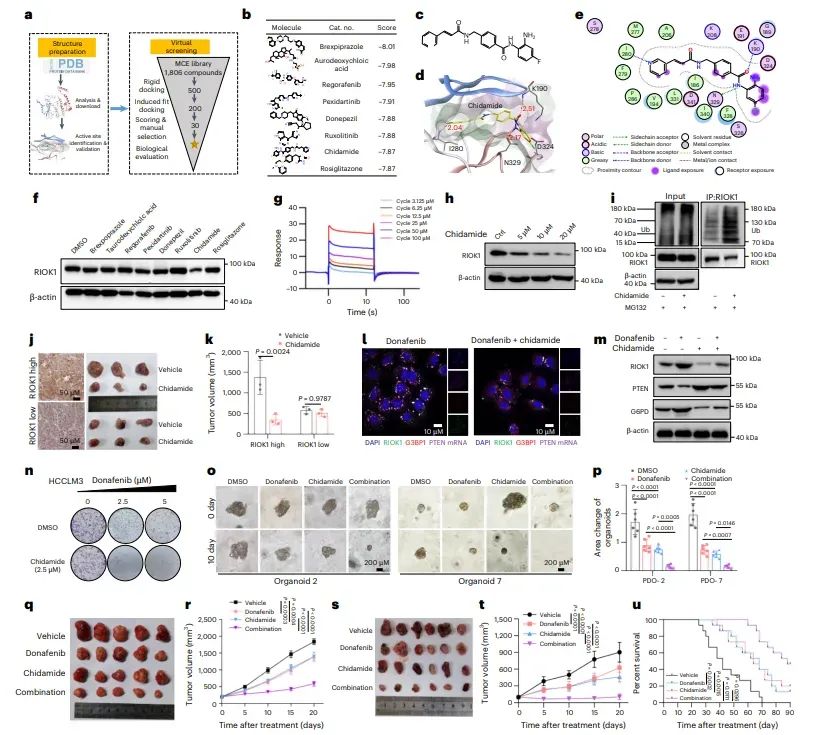
8、RIOK1 与 TKI 耐药及不良预后相关
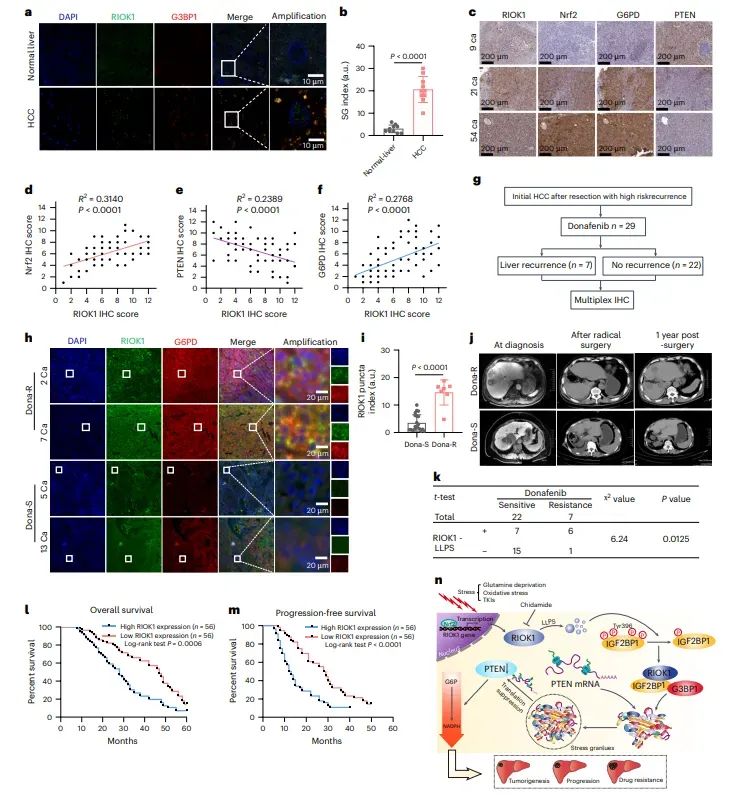
文章小结
本研究聚焦于肝细胞癌(HCC)中RIOK1(一种非典型激酶)的作用及其机制。研究通过生信分析发现RIOK1在HCC中高表达,并与不良预后相关。RIOK1通过液-液相分离(LLPS)与IGF2BP1和G3BP1相互作用,形成应激颗粒(SGs),从而捕获PTEN mRNA并抑制其翻译,激活磷酸戊糖途径(PPP),帮助细胞应激解决并抵抗酪氨酸激酶抑制剂(TKI)的毒性。此外,研究还发现小分子抑制剂chidamide能够下调RIOK1,增强TKI的疗效,为HCC治疗提供了新的策略。
LLPS过程广泛存在于细胞核、细胞质和细胞器中,是许多细胞过程的重要组成部分,也是无膜细胞器(MLOs)形成的主要机制。液-液相分离(LLPS)在人体内通过组织无膜细胞器(如应激颗粒、核仁)来调控信号传导、基因表达等生命活动,维持细胞稳态。基于细胞内的分子机制和动态调控,是现在研究疾病新机制的一大潮向,我们可为您提供基础科研相关的课题思路和技术服务,解决您在临床研究中的表型新机制问题。只要有想法,右上角联系小编,课题指导/方案设计/定制分析/实验验证这里应有尽有~






